结构化学章节内容
2026-02-07 17:39:12
离子晶体是由电负性差别很大的两种或几种元素形成的化合物。一方面,由典型的金属元素,失去一个或多个电子形成正离子,另一方面由典型的非金属获得等价的电子形成负离子。正负离子由库仑力(静电力)相互结合在一起,这种化学键称离子键,库仑力与正负离子电荷成正比,与正负离子间距成反比。
我们可用晶格能来表示离子键的强弱。首先讨论晶格能的静电模型。若两个离子各带电荷q1e和q2e(视为点电荷),两者相距r,则静电库仑势
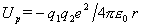
负号表示两个离子电荷符号相反,导致离子间相互吸引。在晶体中,必需考虑所有N个离子间的相互作用
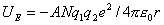
A是晶体结构类型的参数,1918年由Madelung提出,所以称Madelung常数。
括号内的多项式趋近于1.74756……,即NaCl型晶体的Madelung常数。
![]()
离子间相距一定距离r而不能无限接近,是因为离子间的电子云存在着斥力。Born假设,两个离子间的排斥力可用B/rn来表示,B与n是实验难以测定的常数,这样晶格能的负值可由下式给出:


